Управление pH в гидропонике с использованием только электричества — Наука в гидропонике
![]()
![]()
![]()
![]()
Способность растений усваивать питательные вещества изменяется в зависимости от рН. Это делает поддержание рН питательных растворов в приемлемом диапазоне — чаще всего от 5,8 до 6,2 — одной из самых важных задач в гидропонных культурах. Обычно это делается с добавлением сильных кислот или оснований для уменьшения или увеличения pH, когда он отклоняется от предполагаемого значения. Это требует либо ручного контроля с тщательным добавлением этих веществ, либо автоматизированных процессов с использованием насосов, чтобы гарантировать, что pH всегда остается на правильном уровне. Однако обоим этим методам не хватает точного контроля, они требуют тщательного обслуживания и контроля и могут привести к дорогостоящим ошибкам. Сегодня я хочу обсудить альтернативный метод, основанный на совершенно иной идее контроля pH, на идее о том, что мы можем окислять или восстанавливать воду с помощью электричества для изменения pH. Да, вы можете изменить pH, используя буквально только электричество..

Начнем с обсуждения pH и того, как он меняется. pH раствора рассчитывается как -Log(|H+|) где |Н+| — молярная концентрация H+ ионы в растворе. В воде константа диссоциации 1×10-14 (при 25C), всегда нужно соблюдать, поэтому мы всегда знаем, что произведение |H+| и |ОН–| должен дать нам этот номер. Когда вы добавляете кислоты, вы увеличиваете |H+| наоборот |ОН–| уменьшается, и pH снижается, когда вы добавляете основания |OH-| увеличивается, |Н+| снижается, а рН повышается. Проще говоря, все, что вам нужно для снижения pH, — это источник H.+ и все, что вам нужно для повышения pH, является источником OH–.
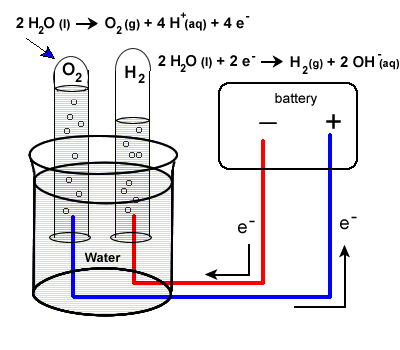
Именно здесь электрохимия дает нам самое простое решение, на которое мы только могли надеяться. Вода может быть окислена или восстановлена. Когда вы пропускаете через воду ток — выше минимально необходимого напряжения — вода расщепляется на молекулы водорода и кислорода. На изображении ниже вы можете видеть, как реакция окисления воды генерирует ионы H+, а реакция справа генерирует ионы OH-. Когда вы делаете это в одной ячейке, как показано ниже, ионы H+, образующиеся на аноде, реагируют с ионами OH-, образующимися на катоде, и pH раствора остается нейтральным, в то время как на аноде образуется кислород, а на катод.
Однако мы можем использовать ионообменные мембраны для разделения этих двух процессов, что позволяет нам контролировать, где происходит каждая реакция и где образуется кислота или основание (предотвращая их простое смешивание и нейтрализацию). На самом деле все, что нам нужно, это иметь электрод в нашем питательном растворе и еще один электрод во вспомогательной ячейке, отделенной от нашего питательного раствора ионообменной мембраной. Эта концепция на самом деле не нова и уже была предложена в статье 1998 года для контроля pH в гидропонных системах. Хотя его никогда не пробовали в производственной системе, все концепции были проверены и продемонстрировали адекватную работу в тестовых решениях.
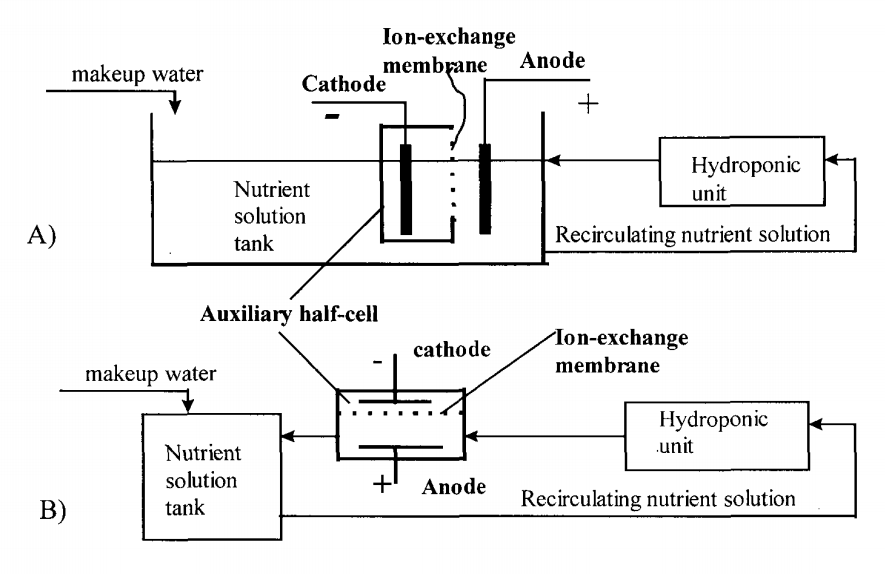
Одна из больших проблем этой установки заключается в том, что катодная сторона включает выделение газообразного водорода, что может быть опасно, но его можно полностью избежать, заменив катодную полуреакцию гораздо более безвредной химией. В качестве примера, также предложенного в статье выше, вы можете заменить полуэлемент катода раствором сульфата меди с медным электродом и анионообменной мембраной. Это позволит вам, чтобы ваша реакция восстановления была восстановлением меди на медном месте, что является очень простой реакцией. Поскольку мембрана обменивается только анионами, в ваш питательный раствор попадет только сульфат, который является безопасным анионом в гидропонной культуре. Это, конечно, означает, что ваш полуэлементный электрод и раствор необходимо будет заменить со временем, но это совершенно не зависит от процесса управления (гораздо больше похоже на заправку газового баллона). Анод будет выделять только кислород в вашем питательном растворе, что является потенциально полезным побочным эффектом.
Однако использование полуэлемента из сульфата меди ограничило бы систему управления более низким pH, но это не проблема, поскольку это наиболее часто используемая операция в гидропонике (людям очень редко приходится повышать pH своих растворов). Если на стороне катода используется надлежащая система вентиляции или система каталитической рекомбинации, вы также можете пойти по простому пути окисления/восстановления воды и иметь возможность увеличивать или уменьшать pH, используя в основном чистое электричество.
Я определенно планирую построить одну из этих установок в будущем. В сочетании с современными датчиками и микроконтроллерами это позволяет очень легко поддерживать очень точный контроль над pH раствора, компенсируя в режиме реального времени все изменения pH, производимые растениями, без риска чрезмерной или недостаточной компенсации ( как это происходит, когда вы используете кислотно-щелочные добавки).