Сохранение стабильного уровня pH вашего гидропонного питательного раствора — Наука в гидропонике
![]()
![]()
![]()
![]()
Кошмаром для многих гроверов в гидропонной индустрии является тот факт, что время от времени необходимо вносить коррективы в питательные растворы. На самом деле люди часто регулируют pH своих питательных растворов несколько раз в неделю, чтобы поддерживать значения, близкие к тем, которые считаются идеальными. Тем не менее, большинство производителей не знают об основных фактах, связанных с изменениями pH, и о том, как их можно избежать (пожалуйста, обратитесь к часто задаваемым вопросам о pH для получения дополнительной информации).
Одним из способов эффективного контроля этого изменения pH является добавление вещества, которое уравновешивает этот заряд и обеспечивает реакционную способность по отношению к соединениям OH(-) или H3O(+). Такое добавление веществ в раствор для защиты химического равновесия от изменений pH называется «буферизацией». В гидропонике растворы чаще всего «забуфериваются» с помощью аммиака, однако мы можем провести моделирование, чтобы увидеть, как эти два иона действуют против «кислотных» или «щелочных» добавок, и увидеть, как на это реагирует вся гидропонная система.
Моделирование выполняется с использованием программного обеспечения Maxima, и все системы уравнений генерируются в соответствии с уравнениями равновесия, уравнениями баланса массы и уравнениями баланса заряда (это называется систематическим исследованием химического равновесия). Концентрации всех буферных агентов составляли 0,1 мМ.
Короче говоря, на приведенном ниже графике показаны результаты моего моделирования добавления «кислоты» или «основы» с использованием трех разных буферных агентов. Синяя линия показывает изменение при использовании лимонной кислоты/цитрата в качестве буферного агента, оранжевая линия показывает, когда в качестве буферного агента используется аммиак, а желтая линия показывает, когда в качестве буферного агента используется карбонат/лимонная кислота.
–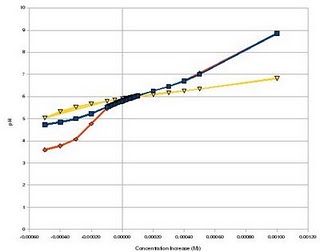 –
–
Как видно, цитрат обеспечивает очень хорошую буферную способность по отношению к кислым значениям рН, в то время как его буферный потенциал по отношению к щелочным значениям рН становится меньше. Аммиак практически не обладает буферным потенциалом по отношению к кислым значениям рН, в то время как он обеспечивает почти такой же буферный эффект по отношению к основным значениям рН, как лимонная кислота. Обратите внимание, что базовое буферирование pH кажется одинаковым для обоих буферов, потому что здесь влияние ионов фосфата внутри раствора становится более заметным.
–
Однако, когда карбонат/лимонная кислота используется в качестве буферного агента, буферная способность раствора резко возрастает как в сторону кислых, так и в сторону щелочных значений pH, что становится чрезвычайно высоким. Тем не менее, следует ожидать, что раствор с этой буферной смесью прослужит в несколько раз дольше, чем обычный раствор, без необходимости каких-либо корректировок pH. На практике приготовление этого раствора дало мне по крайней мере три недели потребления растений без необходимости корректировки pH.